
|

| 产地 | 武汉 |
| 品牌 | 摩科MOLCOO |
| 货号 | M066003 |
| 用途 | 药物科研 |
| 包装规格 | 20-500MG |
| 纯度 | 98% |
| CAS编号 | |
| 是否进口 | 否 |
| 产品编号: | M066003 |
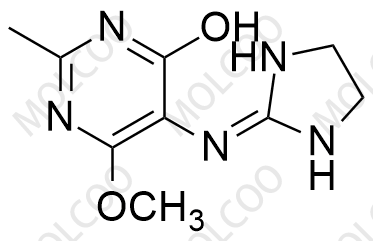
| 英文名: | Moxonidine EP Impurity C |
| 英文别名: | 5-(imidazolidin-2-ylideneamino)-6-methoxy-2-methylpyrimidin-4-ol |
| CAS号: | 352457-34-2 |
| 分子式: | C9H13N5O2 |
| 分子量: | 223.23 |
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223
在药物研发及仿制药一致性评价过程中,杂质控制是确保药品质量和临床安全性的核心环节。莫索尼定为嘧啶类化合物,化学名为4-氯-N-(4,5-二氢-1H-咪唑-2-基)-6-甲氧基-2-甲基-5-嘧啶胺盐酸盐。其合成以乙脒盐酸盐为原料,经环合、硝化、氯化、还原、加成脱水、醇解成盐等多步反应制得。合成过程中易产生工艺杂质和降解杂质,主要杂质类型包括:未反应的中间体(如2-甲基-4,6-二氯-5-氨基嘧啶)、副反应产物(如缩合物、双甲氧物)以及水解降解产物等。
研究进展: 已有研究者采用2-甲基-4,6-二氯-5-氨基嘧啶为起始原料,经与N-乙酰基-2-咪唑烷酮缩合、水解制备了莫索尼定杂质A和杂质B两个有关物质,杂质A和杂质B总收率分别为44.8%和45.5%,纯度均高于99.2%(HPLC法),可作为莫索尼定药物质量控制的杂质对照品。目前已有文献采用HPLC内标法测定盐酸莫索尼定片含量、含量均匀度,并对原料生产过程中引入的缩合物及双甲氧物两种杂质进行了考察,测定了杂质的最低检出限量。
齐全的杂质谱系可帮助研发人员解析杂质生成路径、优化合成关键工艺参数、建立稳健的质量控制方法,确保产品符合国内外法规标准,规避研发与上市风险。
产品核心优势
杂质谱系全面:覆盖莫索尼定EP药典杂质(EP杂质A/B/C/D)、工艺杂质、降解杂质等全系列杂质对照品,满足原料药及制剂研发、仿制药一致性评价、ANDA注册申报等多场景需求。
高纯度保障:核心杂质对照品纯度普遍≥95%,部分产品纯度可达98%~99%以上,批次间稳定性良好,满足痕量杂质的精准定量分析要求。
图谱资料齐全:随货提供COA、¹H-NMR、¹³C-NMR、MS、HPLC等结构确证图谱及纯度证明资料,还可根据客户要求提供红外、紫外、TGA、QNMR、二维谱等额外图谱,为注册申报提供完整数据支撑。
结构确证严谨可溯源:采用多种谱学手段联合确证,报告符合NMPA、FDA、EMA、EP等国内外药监机构申报要求,保障数据的可追溯性。部分供应商已通过ISO17034国际标准物质生产者能力体系认证。
灵活规格选择:提供10mg/25mg/50mg/100mg/1g等多种包装规格,适配研发小试、中试放大及批量化检测等不同阶段需求。
现货供应,快速响应:常年备有稳定现货库存,顺丰发货,1~2周内到货,确保研发进度不受供货周期影响。
莫索尼定杂质对照品广泛适用于以下场景:
- 新药研发与仿制药一致性评价:杂质谱解析、嘧啶环构建及咪唑烷酮缩合工艺优化、原研药杂质谱对标分析
- 质量研究与标准制定:有关物质方法学验证(HPLC/LC-MS)、质量控制体系建立
- 稳定性研究:长期稳定性及加速稳定性试验中的杂质监测、降解产物研究
- 注册申报:符合国内外药监机构ANDA/NDA申报要求
- 药典标准符合性研究:满足EP药典杂质A/B/C/D专项控制要求
湖北摩科优势
- 深耕药物杂质领域多年,拥有丰富的杂质对照品研发与生产经验
- 产品库丰富,涵盖莫索尼定EP药典杂质、工艺杂质、降解杂质等全品类
- 质量体系完善,出库产品均经严格检测(LCMS+HPLC),确保数据真实可靠
- 技术支持专业,提供化合物定制合成及制备分离纯化服务
- 售后响应及时,专业团队全程跟进,解决客户疑问
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223