
|

| 产地 | 武汉 |
| 品牌 | 摩科MOLCOO |
| 货号 | A051025 |
| 用途 | 药物科研 |
| 包装规格 | 20-500MG |
| 纯度 | 98% |
| CAS编号 | |
| 是否进口 | 否 |
| 产品编号: | A051025 |
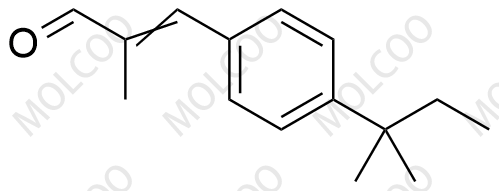
| 英文名: | Amorolfine Impurity 25 |
| 英文别名: | 2-methyl-3-(4-(tert-pentyl)phenyl)acrylaldehyde |
| CAS号: | 67468-55-7 |
| 分子式: | C15H20O |
| 分子量: | 216.32 |
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223
阿莫罗芬(Amorolfine)由德国霍夫曼·拉罗氏公司研发,是一种吗啉类局部外用药物,于1991年在英国首次获批上市。近年来,盐酸阿莫罗芬制剂研发持续升温。2025年,盈科生物与北京福元药业的盐酸阿莫罗芬搽剂相继获批上市;同年3月,恒瑞医药盐酸阿莫罗芬搽剂以仿制4类报产。目前国内已有江苏福邦药业和武汉诺安药业2家盐酸阿莫罗芬乳膏仿制药上市。从内部数据看,国内有不下10家企业在开展盐酸阿莫罗芬品种的研发与申报工作。
在药物研发及仿制药一致性评价过程中,杂质控制是确保药品质量和临床安全性的核心环节。阿莫罗芬的合成工艺涉及多步反应,杂质类型涵盖工艺杂质、降解杂质及手性异构体等多种类别。阿莫罗芬分子中含有一个手性吗啉环和一个手性侧链,合成过程中易产生多种非对映异构体杂质。《欧洲药典》对盐酸阿莫罗芬原料药及制剂中的有关物质提出了明确的质量控制要求,对杂质D、杂质E、杂质I、杂质J、杂质M等多个特异性杂质进行了限定。
齐全的杂质谱系可帮助研发人员解析杂质生成路径、优化合成工艺参数、建立稳健的质量控制方法,确保产品符合国内外法规标准,规避研发与上市风险。
产品核心优势
杂质谱系全面:覆盖阿莫罗芬工艺杂质、降解杂质、手性异构体、非对映异构体混合物及EP特异性杂质(杂质A、B、C、D、E、I、J、M、O等)全系列杂质对照品,满足原料药及制剂研发、仿制药一致性评价、注册申报等多场景需求。
高纯度保障:核心杂质对照品纯度普遍≥95%,部分产品纯度可达98%以上,批次间稳定性良好,满足痕量杂质的精准定量分析要求。
图谱资料齐全:随货提供COA、¹H-NMR、¹³C-NMR、MS、HPLC等结构确证图谱及纯度证明资料,还可根据客户要求提供红外、紫外、TGA、QNMR等额外图谱,为注册申报提供完整数据支撑。
结构确证严谨可溯源:采用多种谱学手段联合确证,精准表征手性构型及非对映异构体比例,报告符合国内外药监机构申报要求,保障数据的可追溯性。
灵活规格选择:提供10mg/25mg/50mg/100mg等多种包装规格,部分杂质可提供更大规格,适配研发小试、中试放大及批量化检测等不同阶段需求。
现货供应,快速响应:常年备有稳定现货库存,顺丰发货,1~2周到货,确保研发进度不受供货周期影响。
阿莫罗芬杂质对照品广泛适用于以下场景:
- 新药研发与仿制药一致性评价:杂质谱解析、吗啉环构建工艺优化、原研药杂质谱对标分析
- 质量研究与标准制定:有关物质方法学验证(HPLC/GC-MS)、质量控制体系建立
- 稳定性研究:长期稳定性及加速稳定性试验中的杂质监测、特定杂质溶液稳定性研究
- 注册申报:符合国内外药监机构申报要求
- 手性杂质控制:满足非对映异构体杂质限度的精准定量分析要求
湖北摩科优势
- 深耕药物杂质领域多年,拥有丰富的杂质对照品研发与生产经验
- 产品库丰富,涵盖阿莫罗芬EP药典杂质、工艺杂质、降解杂质、手性异构体及非对映异构体等全品类
- 质量体系完善,出库产品均经严格检测(LCMS+HPLC),确保数据真实可靠
- 技术支持专业,提供化合物定制合成服务
- 售后响应及时,专业团队全程跟进,解决客户疑问
更多杂质项目需求,欢迎联系:
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223