
|

| 产地 | 武汉 |
| 品牌 | 摩科MOLCOO |
| 货号 | C010004 |
| 用途 | 用于新药申报及研究 |
| 包装规格 | 10mg/15mg/20mg/25mg |
| 纯度 | 98% |
| CAS编号 | 32830-01-6 |
| 是否进口 | 否 |
| 产品编号: | C010004 |
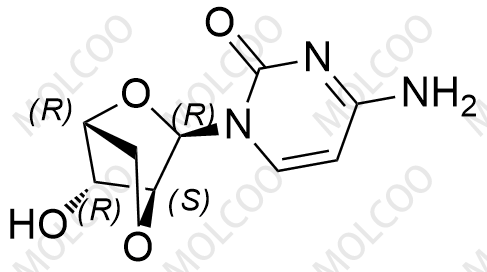
| 英文名: | Cytarabine Impurity 4 |
| 英文别名: | 阿糖胞苷EP杂质F;Cytarabine EP Impurity F;4-amino-1-((1R,3R,4S,7R)-7-hydroxy-2,5-dioxabicyclo[2.2.1]heptan-3-yl)pyrimidin-2(1H)-one |
| CAS号: | 32830-01-6 |
| 分子式: | C9H11N3O4 |
| 分子量: | 225.20 |
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223
随着对核苷类药物质量要求的不断提高,阿糖胞苷原料药及制剂中的已知杂质已成为药企杂质谱研究及注册申报的核心关注点。
产品纯度:≥95% ~ ≥97%
产品规格:10mg / 25mg / 50mg / 100mg(可定制更大包装)
供货状态:现货供应,货期1-2周
阿糖胞苷作为一种核酸类似物药物,其杂质研究是药品质量控制的核心环节。杂质可能在工艺步骤中引入(如起始物料中的相关物质)或在储存过程中形成(如水解和氧化等应激条件下的降解产物)。典型降解途径包括胞嘧啶-阿拉伯糖苷键的水解断裂、胞嘧啶环的氧化分解以及核苷骨架内取代基的重排。这些杂质可能影响药物的效力、稳定性和安全性,因此所有杂质均需根据ICH指南进行结构表征和毒理学评估及分析验证。
EP杂质A为阿糖胞苷的脱氨基降解产物,是稳定性研究中需重点监控的关键杂质。EP杂质C(胞嘧啶)和EP杂质D(尿嘧啶) 为核苷骨架裂解产生的小分子碱基杂质,既是合成起始物料中可能残留的工艺杂质,也是药物降解过程中的标志性产物。EP杂质E(胞苷) 为阿糖胞苷的差向异构体,属于合成工艺中的关键异构化杂质。EP杂质F(5-甲基胞苷) 为阿糖胞苷的同系物杂质,同样是重要的合成副产物。
因此,对阿糖胞苷EP杂质系列进行系统研究和严格控制,不仅是药典合规的基本要求,更是保障临床用药安全性和药品质量稳定性的核心环节。
应用场景:
阿糖胞苷杂质对照品作为经过全面表征的化学化合物,可作为原料药阿糖胞苷的参考标准,应用于药物研发的多个关键环节:
分析方法开发与验证(AMV) —— 作为已知杂质的定性、定量标尺,用于建立和验证HPLC、LC-MS/MS等分析方法。
ANDA与DMF申报 —— 在ANDA申报或DMF备案中,需对原料药中的已知杂质进行完整的定性与定量控制。
生产过程中的质量控制(QC) —— 在阿糖胞苷原料药及制剂生产的中控和放行检测中,用于监控各EP杂质的含量水平。
稳定性研究 —— 用于考察阿糖胞苷原料药或制剂在加速或长期稳定性试验中各杂质的变化趋势。
杂质谱分析与遗传毒性评估 —— 协助企业建立完整的杂质谱数据库,为杂质的安全性评价和限度制定提供科学依据。
科学研究 —— 阿糖胞苷杂质及其相关化合物可用于核苷代谢通路、DNA合成抑制等基础研究领域。
产品核心优势
EP杂质系列全覆盖:提供阿糖胞苷EP杂质A~I全系列对照品及多种非药典级杂质,满足药典杂质谱研究的完整需求。阿糖胞苷EP杂质对照品严格符合欧洲药典(EP)规范,所有可溯源至EP的物质均附带经验证的分析数据,包括纯度、结构确认和光谱表征。
高纯度保障:产品纯度可达95%~97%以上,经严格的分析检测验证。随货提供COA、HPLC、H-NMR、MS等检测图谱,满足基本分析需求;可根据客户需求提供C-NMR、红外、紫外、水分数据、定量核磁、二维谱等额外检测服务。
规格灵活,按需选择:提供10mg、25mg、50mg、100mg等多种包装规格,满足研发、中试及申报各阶段的用量需求。
稳定供应,快速交付:现货供应,货期2-3周,支持紧急需求下的快速响应。
欢迎咨询合作:
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223