
|

| 产地 | 武汉 |
| 品牌 | 摩科MOLCOO |
| 货号 | K005026 |
| 用途 | 用于新药申报及研究 |
| 包装规格 | 20-500MG |
| 纯度 | 98% |
| CAS编号 | |
| 是否进口 | 否 |
酮洛芬(Ketoprofen)作为一种经典的芳基丙酸类非甾体(NSAID),自1967年获得专利、1980年获准医疗使用以来,其口服、外用凝胶及注射制剂在全球市场占有重要地位。随着国内外药典标准及ICH指南对有关物质控制的持续加强,酮洛芬原料药和制剂中杂质的系统研究已成为药企合规申报和质量管控的核心议题。我们提供符合标准的酮洛芬杂质系列对照品,为客户分析方法开发、质量控制及注册申报提供精准可靠的解决方案。
产品名片
酮洛芬杂质26
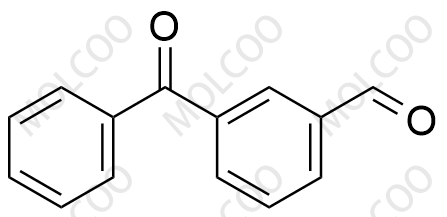
| 产品编号: | K005026 |
| 英文名: | Ketoprofen Impurity 26 |
| 英文别名: | 3-benzoylbenzaldehyde |
| CAS号: | 71856-95-6 |
| 分子式: | C14H10O2 |
| 分子量: | 210.23 |
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223
储存条件:常温避光保存,部分杂质建议低温(-20°C)保存
规格:10mg / 25mg / 50mg / 100mg(可定制更大包装)
纯度:≥95% ~ ≥99%(依不同杂质品种而异,高纯度杂质A可达99.86%)
湖北摩科产品核心优势
杂质系列全覆盖:提供酮洛芬EP杂质A~L全系列对照品(包括杂质A至杂质L等多种类型),满足药典杂质谱研究的完整需求。
高纯度保障与配套资料齐全:产品纯度可达95%~99%以上,随货可提供COA、HPLC纯度图谱、H-NMR、MS(质谱)、红外光谱等多种检测数据,满足基本申报要求。可根据需求进一步提供C-NMR、TGA、KF水分测定、定量核磁(QNMR)、二维核磁(2D-NMR)、UV紫外光谱、热重分析等深度分析服务。
多规格选择,灵活供给:提供10mg、25mg、50mg、100mg等多种包装规格,可定制1g以上大包装,满足研发、中试放大及正式注册申报各阶段的差异化用量需求。
稳定供应,快捷交付:现货库存充足,正常货期2-3周,为紧急需求提供快速响应通道,确保项目进度不延误。
专业团队与研发平台支撑:公司拥有标准化有机合成实验室和先进的仪器分析平台,配备LC-MS/MS、LC-MS、HPLC、GC、TGA、KF等多套大型检测设备。90%以上为经验丰富的专业技术人才,能够提供药物杂质定制合成、工艺杂质优化、未知杂质的分离制备与结构鉴定、以及杂质对照品的全面标化服务,助力客户应对复杂杂质研究挑战。
酮洛芬杂质的产生可能来源于合成工艺、降解途径和不适当的储存条件等多种因素。在酮洛芬原料药和制剂生产过程中,需对工艺杂质(如原料中残留的Ketoprofen EP Impurity A等合成中间体杂质)、降解产物(如水解或氧化产物)以及潜在遗传毒性杂质进行系统识别与控制。其中,酮洛芬EP杂质A是合成过程中的重要中间体杂质,也是光降解产物——研究表明经光照后杂质A会明显增加。
EP杂质A(CAS 66067-44-5)为1-(3-苯甲酰基苯基)乙酮,ICH Q3A指南推荐的报告限为0.1%(1000 ppm)。它不仅是有机杂质,还是关键的已知降解产物,在酮洛芬原料药及制剂的有关物质检查中须重点监控和定量分析。针对酮洛芬注射液中六种有关物质的同步测定方法已被开发,并通过HPLC在C18柱(4.6mm×250mm)上进行分离。
EP杂质C(CAS 68432-95-1)为3-羧基-α-甲基苯乙酸,也是酮洛芬USP相关化合物C,属降解类杂质,需常规监控。EP杂质F(CAS 42872-30-0)为腈类已知杂质,不仅是有机杂质,也可能为残料溶剂引入的遗传毒性风险杂质。该杂质可作为参考标准,并可根据可行性提供针对药典标准的进一步可追溯性,完全符合监管指南的详细表征数据要求。
EP杂质L(CAS 1797984-80-5)为消旋-2',4',5'-三甲基酮替芬,是EPA合成工艺中产生的立体异构体杂质,需严格限控纯度。EP杂质E为相关酰胺类杂质,EP杂质D属甲酯类杂质,也均须通过HPLC和MS等分析技术进行杂质的定性定量分析。EP杂质B为工艺残留物,EP杂质G为酯交换杂质,均需保持监测以符合药典。
因此,对酮洛芬EP杂质系列进行全面且系统的控制,是符合药典合规要求、保障用药安全及通过ANDA/DMF申报的关键。
酮洛芬杂质对照品作为具备全面表征数据和药典溯源性的参考标准品,适用于药物研发与质量控制的全周期:
分析方法开发与验证(AMV) :可作为已知杂质定性与定量标准,用于建立和验证高效液相色谱(HPLC)、液相色谱-质谱联用(LC-MS)等分析方法的专属性、灵敏度与准确性。酮洛芬EP杂质F可用于分析方法开发和验证。对于注射剂类产品,相关研究人员已采用RP-HPLC法同时测定六种有关物质,实现了同步高效分离。
ANDA与DMF申报:在中美双报时,必须遵循ICH Q3A/Q3B和USP/EP药典标准,对原料药中所有已知杂质进行系统的定性、限度研究和定量控制。酮洛芬EP杂质对照品可作为符合监管法规要求的实物依据,满足申报资料的完整性要求。
生产过程中的质量控制(QC) :在酮洛芬原料药及制剂生产的中控和放行检测中,通过外标法对各EP杂质进行定量,确保产品质量符合法定标准。典型限度要求为:单个已知杂质≤0.2% ~ 0.5%,总杂质一般不超过1.0%。对于注射剂产品,杂质控制更为严格。
稳定性研究:用于考察酮洛芬原料药和制剂在加速或长期稳定性试验中EP杂质(如杂质A、杂质E)的变化趋势。在光、热、湿度等因素影响下,杂质A的含量可能会增加,监控其降解行为可为药品的有效期评估提供关键数据依据。
杂质谱分析与遗传毒性评估:协助制药企业建立完整的杂质谱数据库,对可能存在的遗传毒性杂质(如杂质F)进行风险评估,并制定严格的控制策略。
科学研究:酮洛芬杂质及相关化合物可用于NSAID类药物的代谢通路、杂质毒理学评价以及药物降解机理等基础研究。
我们深知杂质研究是药物质量控制的生命线,通过全面、精准的杂质对照品和技术支持,帮助客户轻松应对复杂的杂质谱分析和合规申报挑战。
无论您是进行酮洛芬原料药的杂质谱研究、制剂的质量控制体系建设,还是准备ANDA/DMF申报材料,我们的酮洛芬杂质对照品都将成为您手中最可靠的质控标尺和申报利器。
欢迎与我们联系,咨询产品价格、库存情况、技术参数或定制合成需求。我们期待与您携手,共同为酮洛芬系列药品的质量和安全保驾护航!
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223