
|

| 产地 | 武汉 |
| 品牌 | 摩科MOLCOO |
| 货号 | M076020 |
| 用途 | 药物科研 |
| 包装规格 | 20-500MG |
| 纯度 | 98% |
| CAS编号 | 206269-25-2 |
| 是否进口 | 否 |
| 产品编号: | M076020 |
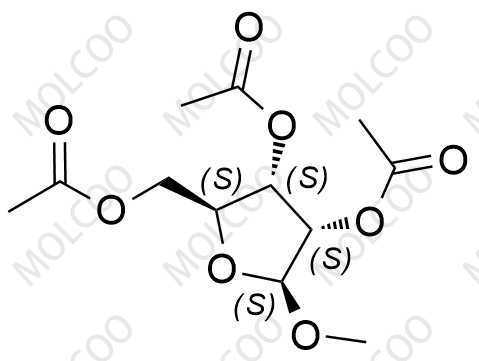
| 英文名: | Maribavir Impurity 20 |
| 英文别名: | (2S,3S,4S,5S)-2-(acetoxymethyl)-5-methoxytetrahydrofuran-3,4-diyl diacetate |
| CAS号: | 206269-25-2 |
| 分子式: | C12H18O8 |
| 分子量: | 290.27 |
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223
马立巴韦是CMV pUL97激酶抑制剂,于2021年在美国获批上市。2025年12月中国《临床急需境外新药名单》也已正式收载本品,国内仿制研发与一致性评价工作随之全面启动,杂质谱研究成为质量控制的焦点。
随着马立巴韦仿制药研发热潮兴起,其原料药及制剂中的已知杂质已成为药企杂质谱研究和DMF申报的核心关注点。我们为您提供马立巴韦全套杂质对照品,涵盖工艺杂质、降解产物及亚硝胺类遗传毒性杂质,为药物分析方法开发、质量控制和注册申报提供精准的实物标尺。
储存条件:-20°C低温避光保存
产品纯度:≥95% ~ ≥99%
产品规格:10mg / 20mg / 25mg / 50mg / 100mg / 500mg(可定制更大包装)
产品核心优势
杂质谱全覆盖:涵盖N-烷基类似物、差向异构体、去糖基化杂质、乙酰化中间体、亚硝胺类遗传毒性杂质等,满足杂质谱研究的完整需求。
高纯度保障:纯度≥95%,核心杂质纯度≥98%,批次间一致性优异。产品经严格的分析检测验证,配备LC-MS/MS、HPLC、GC、NMR、QNMR定量、TGA热重等先进设备完成结构确证。
多规格可选:提供10mg、20mg、25mg、50mg、100mg、500mg等多种包装规格,满足研发、中试及申报各阶段的用量需求,支持毫克至克级定制合成。
配套资料齐全:随货提供COA、HPLC、H-NMR、MS等检测图谱,满足基本分析需求;可根据客户需求提供C-NMR、IR、UV、水分数据、定量核磁、二维谱等额外检测服务。
稳定供应,快速交付:现货供应,当日发货,货期1-2周,支持紧急需求下的快速响应。
为什么马立巴韦杂质值得高度关注?
一、药政监管下,杂质研究是仿制药研发的“入场券”
马立巴韦的核心化合物专利US 8158628将于2025年11月前后到期,各仿制药企业已提前进入研发储备阶段。杂质研究作为仿制药“质量一致性评价”的核心技术标准,直接决定了制剂能否与原研药实现质量等效。马立巴韦分子含有苯并咪唑母核与呋喃糖环,合成路线涉及苯并咪唑环构建、糖苷键形成和侧链胺化等多步反应,易产生N-烷基类似物、差向异构体、去糖基化产物等工艺杂质;同时,马立巴韦结构中的仲胺基存在形成亚硝胺类遗传毒性杂质的风险。
已收载于NMPA《临床急需境外新药名单》(2025年12月版):表明本品价值已获官方认可,国内上市审评路径进一步明确,推动仿制药研发进程提速。
二、杂质谱全览:从工艺中间体到降解产物的完整覆盖
N-烷基类似物杂质:马立巴韦侧链为异丙氨基(-NH-CH(CH₃)₂),合成中可能产生N-甲基和N-乙基取代的类似物(CAS 176161-46-9、176161-49-2),这些为一类关键工艺相关杂质,直接影响API纯度,须在有关物质检查中严格监控。
差向异构体/立体异构杂质:糖苷键形成过程中可能存在立体构型错误,产生C2'/C3'/C4'位差向异构体和β→α异头异构化产物(如杂质8,CAS 462114-04-1),这类杂质与主成分结构高度相似,色谱分离难度大,是对分析方法开发提出的关键挑战。
工艺中间体和去糖基化杂质:苯并咪唑游离母核(杂质11,CAS 176161-55-0)是关键的起始物料引入杂质和去糖基降解产物,可直接反映合成路线和工艺稳定性。全乙酰化中间体是马立巴韦合成路线的关键工艺中间体残留杂质,其残留水平反映了工艺路线中最后一步脱保护反应的完成度及纯化效果。
亚硝胺类遗传毒性杂质(N-亚硝基马立巴韦):马立巴韦分子含有仲胺结构,在合成工艺或辅料引入)条件下,存在形成N-亚硝胺类遗传毒性杂质的潜在风险。追踪USP、EMA、JP、BP标准,该杂质可在原料药和制剂环节以痕量水平存在,须采用高灵敏度检测方法进行系统评估和控制。
其他非药典杂质/降解产物:作为工艺与降解双源杂质,具有独特的色谱保留特征和高分辨率质谱指纹。非药典杂质对照品自主研发的已知工艺副产物和降解产物库,为企业建立更全面的杂质谱管控提供了额外标尺。
因此,对马立巴韦杂质进行系统研究和严格控制,既是满足法规申报的刚性要求,更是保障药品安全性的核心防线。
应用场景:
马立巴韦杂质对照品作为经过全面表征的化合物,可作为原料药马立巴韦的参考标准,广泛应用于以下关键环节:
分析方法开发与验证(AMV):作为已知杂质的定性、定量标尺,用于建立和验证HPLC、LC-MS/MS等检测方法。杂质对照品可用于分析方法开发、方法验证、质量控制或马立巴韦的商业化生产。
ANDA与DMF申报:在ANDA申报或DMF备案中,需对原料药中的已知杂质进行完整的定性与定量控制。马立巴韦杂质对照品可作为参考标准,可根据可行性提供针对药典标准的进一步可追溯性。
生产过程中的质量控制(QC):在马立巴韦原料药及制剂生产的中控和放行检测中,用于监控各工艺杂质和降解产物的含量水平。典型杂质限度要求:单个已知杂质≤0.3%~0.5%,单个未知杂质≤0.1%~0.2%,总杂质≤1.0%~2.0%。
稳定性研究:用于考察马立巴韦原料药或制剂在加速或长期稳定性试验中各杂质的变化趋势,追踪温湿度、光照等条件下杂质变化情况,支撑药物有效期评估和使用储存条件制定。
杂质谱分析与遗传毒性评估:协助企业建立完整的杂质谱数据库,为杂质安全性评价和限度制定提供科学依据。可助力评估原料药和制剂中潜在基因毒性杂质的存在风险。N-亚硝基马立巴韦对照品有助于建立检测限、量化杂质水平,确保痕量亚硝胺杂质控制在FDA和EMA安全限值内。
科学研究:马立巴韦杂质及其相关化合物可用于pUL97激酶抑制剂通路、核苷类似物构效关系等基础研究领域。
无论是马立巴韦原料药杂质谱研究、制剂质量控制,还是ANDA/DMF申报资料准备,马立巴韦杂质对照品都将是您手中精准可靠的质控标尺。
欢迎咨询合作:
湖北摩科——联系人:张玉 电话:18274848843(微信同号) QQ:75037223